نمایش موارد بر اساس برچسب: پرمنگنات پتاسیم
پرمنگنات پتاسیم
پتاسیم پرمنگنات ترکیبی معدنی است با فرمول شیمیایی KMnO۴. نمک آن از یونهای K+ و MnO۴- تشکیل شده است. سابقاً به آن پرمنگنات و پتاش هم میگفتند. پرمنگنات یک مادهٔ اکسندهٔ بسیار قوی است. در آب نیز محلول است و محلولی به رنگ ارغوانی تولید میکند که از تبخیر آن بلورهای منشوری و درخشان به رنگ ارغوانی بسیار تیره (مایل به سیاه) بر جای می ماند. در این ترکیب منگنز باعدد اکسایش ۷+ حضور دارد. توجه: این ماده با گلیسرین واکنش شدیدی میدهد،هیچگاه این دو ماده را کنار هم انبار نکرده و روی یک دیگر نریزید.

محلولی از پتاسیم پرمنگنات در آب درون بالن حجمی
محتویات
۱ساختار و تهیه
۲کاربردها
۲.۱صنایع سینمایی و تلویزیونی
۲.۲تصفیهٔ آب و ضدعفونی
۲.۳کاربردهای زیست پزشکی
۲.۴سنتزهای شیمی آلی
۲.۵تصفیه پسابهای صنعتی
۲.۶عیارسنجی در شیمی تجزیه
ساختار و تهیه[ویرایش]
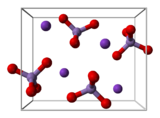
از بلورهایی به شکل اورتورومبیک تشکیل شده که در آن a=910.۵pm و b=572.۰pm و c=742.۵pm است. (a و b و c به ترتیب طول، عرض و ارتفاع دستگاه بلوری اورتورومبیک است.)
همچنین طول پیوند Mn-O در این پیوند برابر ۱۶۲.۹pm است.
تهیهٔ صنعتی پتاسیم پرمنگنات از منگنز دی اکسید است، که خود از سنگ معدن پیرولوسیت به دست می آید. در این روش MnO۲ به دست آمده از پیرولوسیت با پتاسیم هیدروکسید مخلوط شده و در هوا یا در مجاورت پتاسیم نیترات (یک منبع اکسیژن) حرارت داده می شود. در این فرایند پتاسیم منگنات (K۲MnO۴) به دست می آید که در اکسایش الکترولیتی (الکترولیز) در محلول بازی به پتاسیم پر منگنات تبدیل می شود.
| 2 MnO2 + 4 KOH + O2 → 2 K2MnO4 + 2 H2O |
| 2 MnO42– + Cl2 → 2 MnO4– + 2 Cl– |
همچنین پرمنگنات را می توان از اثر دادن سرب دی اکسید (PbO۲) و یا سدیم بیسموتات (NaBiO۳) بر محلول +Mn۲ نیز به دست آورد. از رنگ بنفش روشن حاصل از این واکنش برای تست حضور یا عدم حضور منگنز نیز استفاده می شود.
| پتاسیم پرمنگنات | |
|---|---|
  |
|
| شناسنامه | |
| نام گذاری آیوپاک | پتاسیم منگنات (VII) |
| نامهای دیگر | پتاسیم پرمنگنات پرمنگنات پرمنگنات پتاسیم |
| فرمول شیمیایی | KMnO4 |
| خواص | |
| جرم مولی | 158.034 گرم بر مول |
| نما (ظاهر) | بلورهای سوزنی بنفش مایل به خاکستری |
| رنگ محلول | در محلول دارای رنگ شدید بنفش است که در غلظتهای چند ppm به رنگ ارغوانی در می آید |
| بو | بدون بو |
| چگالی | 2.703 گرم بر سانتیمتر مکعب |
| دمای ذوب | 240oC همراه با تجزیه شدن |
| حلالیت در آب | 6.38 گرم در 100mL آب (در دمای 20oC) 25 گرم در 100mL آب |
| حلالیت | در الکل و حلالهای آلی دیگر تجزیه می شود. |
| ساختار | |
| ساختار بلوری | دستگاه بلوری اورتورومبیک |
| ترموشیمی | |
| آنتالپی استاندارد تشکیل | 813.4- کیلوزول بر مول |
| آنتروپی استاندارد مولی | 171.7 ژول بر کلوین.مول |
| خطرات | |
| MSDS | External MSDS |
| طبقه بندی EU | اکسید کننده(در استفاده احتیاط کنید) مضر برای سلامتی خطرناک برای محیط زیست |



